ASISTENCIA VENTRICULAR EN PEDIATRÍA
Cristina Relaño, Susana Cobos.
Dues, UCIP Hospital General Universitario “Gregorio
Marañón”
INTRODUCCIÓN
La
asistencia ventricular consiste en suplir la función de uno o los dos
ventrículos mediante una bomba mecánica
que restaura la función cardiovascular y el flujo sanguíneo.
La
historia de los dispositivos de asistencia ventricular (VAD) comienza en 1953
cuando Gibbon construye la primera máquina que permite desviar la circulación
cardiopulmonar pudiendo así realizar operaciones a corazón abierto. En la década de los 60 Cooley implantó un corazón
artificial total como puente al trasplante y Bartlett empezó a usar el soporte
circulatorio extracorpóreo en niños con cardiopatías congénitas. Desde entonces
la evolución ha sido constante, desde el balón de contrapulsación hasta la
bomba de rodillo, dispositivos no pulsátiles extracorpóreos uni o
biventriculares con o sin membrana de oxigenación, dispositivos pulsátiles,
implantables, hasta llegar al corazón artificial total.
La
utilización de asistencia ventricular en pacientes pediátricos es un
procedimiento cada vez mas frecuente como consecuencia de las cirugías realizadas en cardiopatías muy
complejas y del aumento de trasplantes
cardiacos pediátricos.
Los
candidatos a la asistencia ventricular proceden de situaciones diferentes:
1. Síndrome
postcardiotomía.
Son pacientes a los que no puede
suprimirse la circulación extracorpórea tras una intervención a corazón
abierto. Esta situación se presenta, afortunadamente, con poca frecuencia en la
cirugía cardiaca pediátrica. Su pronóstico sin ningún tipo de asistencia
mecánica es fatal. La asistencia
ventricular permite reducir el trabajo del miocardio y el consumo de oxigeno,
contribuyendo así a la recuperación metabólica del órgano mientras se mantiene
una adecuada perfusión sistémica.
2. Puente al
trasplante cardiaco
Pacientes con enfermedad cardiaca en
estado final que están en lista de espera para trasplante. En estos casos el
uso del VAD se plantea para mantener las condiciones hemodinámicas del paciente
hasta la aparición de un donante. El problema es la gran escasez de
órganos y el periodo de tiempo
necesario para obtener un órgano adecuado. Este periodo de tiempo es mas
prolongado cuanto menor es el niño.
3. Postrasplante
cardiaco
Pacientes
con fallo del órgano implantado, cuando se presenta un episodio de rechazo
agudo o cuando hay resistencias pulmonares elevadas.
OBJETIVO
Conocer las situaciones clínicas en las que es posible la utilización de este sistema, las
formas de asistencia y los especiales cuidados que requieren los niños que
tienen un dispositivo de asistencia ventricular externa.
Presentar nuestra experiencia.
DISPOSITIVOS
DE ASISTENCIA VENTRICULAR (VAD)
Son
dispositivos mecánicos capaces de bombear sangre sustituyendo la función
ventricular. Los VAD que sustituyen la función del ventrículo derecho sirven como apoyo a la función pulmonar. Los
que sustituyen la función de ventrículo izquierdo apoyan la circulación
sistémica. Su uso puede se uni o biventricular (BVAD).
Existen
diferentes tipos de dispositivos, bomba centrífuga magnética, neumática
pulsátil, rotatoria de rodillo, pulsátil eléctrica, aunque en el presente
trabajo solo vamos a explicar el funcionamiento, manejo y experiencia en
nuestro hospital de la bomba centrífuga magnética BIOMEDICUS Biopump.
 Las
bombas centrífugas magnéticas están constituidas por una carcasa rígida externa
en forma de cono por cuyo vértice se efectúa la entrada de fluido. Dentro de
este cono se disponen otros conos apilados (hasta 3) ,
Las
bombas centrífugas magnéticas están constituidas por una carcasa rígida externa
en forma de cono por cuyo vértice se efectúa la entrada de fluido. Dentro de
este cono se disponen otros conos apilados (hasta 3) ,
los cuales al girar sobre su
propio eje producen
una presión negativa sobre el punto de entrada
y empujan el fluido del circuito
dentro de la bomba.
Una vez que la sangre entra en la cabeza arterial,
la energía cinética es transmitida a la sangre por
los conos rotatorios generando presión en la
bomba y permitiendo que la sangre
se dirija hacia
el punto de salida. En la entrada
y salida del cabezal
de la bomba no existen dispositivos oclusivos.
Si los conos están parados y no rotan la sangre
puede pasar. El flujo que
proporcionan las bombas
centrífugas es de tipo continuo,
no pulsátil.
La
cabeza de la bomba se instala en una consola portátil que dispone de un imán
rotatorio y transmite el movimiento a los conos internos. El sistema
electrónico de la consola nos permite conocer la velocidad de los conos
(revoluciones por minuto). El gasto se calcula a través de un medidor de flujo
situado en la salida del cabezal .
La Biopump es una
consola pequeña y fácil de manejar. Se puede utilizar tanto en adultos como
en niños. Puede girar hasta 5000 rpm y se pueden programar flujos hasta 8
l/min.

ESQUEMA ASISTENCIA VENTRICULAR
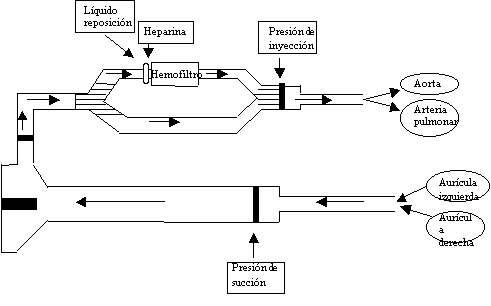
![]()
![]()
FORMAS DE ASISTENCIA VENTRICULAR
Ø
Asistencia ventricular izquierda (LVAD)
La
asistencia izquierda se usa cuando se produce un fallo del corazón izquierdo.
Hay un fracaso del ventrículo izquierdo pero se mantiene la función del
ventrículo derecho. Aparecen síntomas de bajo gasto, aumento del ácido láctico
y disminución de la diuresis, que no mejoran con el tratamiento con inotrópicos, vasodilatadores, diuréticos...... .
La
canulación para poner una asistencia ventricular siempre es transtorácica.
Cuando al paciente no se le puede retirar la circulación extracorpórea después
de una intervención se usan las cánulas ya puestas o bien éstas se cambian de
posición.
Si la
asistencia se pone como puente hasta el trasplante el paciente tendrá que ir al
quirófano para realizarle una esternotomía y colocar las cánulas.
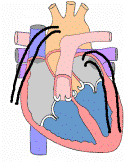
Para asistencia izquierda las
cánulas se ponen en
la aurícula izquierda y la aorta, en la zona del cayado.
Ø
Asistencia ventricular derecha (RVAD)
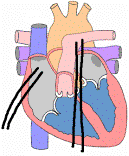 Esta
asistencia se usa cuando hay un fracaso del ventrículo derecho o existen
resistencias pulmonares elevadas que impiden un adecuado flujo pulmonar. El
corazón izquierdo funciona manteniendo la circulación sistémica.
Esta
asistencia se usa cuando hay un fracaso del ventrículo derecho o existen
resistencias pulmonares elevadas que impiden un adecuado flujo pulmonar. El
corazón izquierdo funciona manteniendo la circulación sistémica.
Para asistencia derecha las
cánulas se ponen en
la aurícula derecha y la
arteria pulmonar.
Ø
Asistencia biventricular (BVAD)
Si se
produce un fracaso de los dos ventrículos se puede colocar una asistencia
biventricular. En este caso habría que poner dos bombas con dos sistemas en
paralelo precisando la inserción de cuatro cánulas. Esto plantea serios
problemas en los neonatos y niños pequeños dado su tamaño.
Cuando
hay compromiso pulmonar añadido la mejor opción sería realizar una ECMO ya que
sólo se precisa la inserción de dos cánulas por vía percutánea: yugular interna
dcha. y arteria carótida dcha. El circuito realiza un bypass cardiopulmonar
completo. La sangre venosa sale de la
aurícula dcha. del paciente pasa por el oxigenador de membrana y regresa, oxigenada
y ventilada, a la aorta por la arteria
carótida del mismo lado.
MATERIAL Y
METODOS
Para poder manejar y mantener a este
tipo de pacientes es necesario tener monitorizados y controlados una serie de
parámetros que nos indicaran en todo momento el estado del niño.
MANEJO Y CUIDADOS
DEL PACIENTE CON ASISTENCIA VENTRICULAR
El niño
sometido a asistencia ventricular es un paciente crítico en grave situación
hemodinámica.
Debe tener
monitorizados y controlados una serie de parámetros que nos indicaran en todo
momento el estado del niño:
ECG
La
monitorización de la frecuencia cardiaca nos permitirá detectar alteraciones
del ritmo que pueden repercutir en el funcionamiento del soporte circulatorio y
en la función residual del corazón asistido. Se debe mantener un ritmo sinusal y
una frecuencia cardiaca lo más óptima posible. La FC se mantiene en
valores óptimos calentando o enfriando al paciente y regulando la perfusión de
catecolaminas.
Presión
arterial sistémica (PA)
La PA
media debe mantenerse en los neonatos y lactantes en 40 mmHg y en los
niños mayores alrededor de 60 mmHg para
garantizar una adecuada perfusión renal, esplénica y cerebral.
Con
asistencia ventricular de flujo continuo la curva que aparecerá en el monitor
será sinusoidal
Cuando la
curva de presión arterial comienza a ser pulsátil sin haber modificaciones del flujo de la bomba ni aumento de la
perfusión de catecolaminas es un signo indirecto de recuperación miocárdica.
La
canalización de una arteria nos sirve además
para la extracción de analítica y la medición de gases arteriales.
Presión
aurícula izquierda (PAI)
La PAI
debe mantenerse siempre entre 5 - 15 mmHg para garantizar una adecuada precarga
en el ventrículo izquierdo y optimizar la función residual del órgano.
En LVAD
una presión < 5 mmHg supone una disminución del llenado auricular y la
posibilidad de que la cánula de aspiración auricular cavite creando aire dentro
del circuito. Esto es especialmente importante por las fatales consecuencias
que tendría el embolismo aéreo en el territorio arterial.
Pacientes con RVAD en los que la PAI es > 15 mmHg se
debe suponer un inicio de fracaso del ventrículo izdo. Que precisará un aumento
de los inotrópicos.
La presión baja nos
indicaría que el paciente está hipovolémico, que existe un fracaso en VD o que
el soporte es excesivo (succión auricular alta).
La presión alta indicaría una obstrucción de la cánula, una sobrecarga
de volumen o un soporte inadecuado (flujo bajo).
Presión
venosa central(PVC)
Una PVC
entre 5-15 mmHg nos garantiza una adecuada precarga en el VD.
En RVAD
una presión < 5mmHg supondría una disminución del llenado auricular y la
posibilidad de que la cánula de aspiración auricular cavite creando aire dentro
del circuito.
En
pacientes con asistencia izda y una PVC alta debe sospecharse un fallo
ventricular dcho o una sobrecarga de volumen. Si la presión baja nos indicaría
que hay hipovolemia.
Arteria pulmonar (AP)
La
colocación de un catéter de Saw-Ganz nos permitirá la medición del gasto
cardiaco y la monitorización de la PAP.
La
medición del gasto servirá para modificar los parámetros de la bomba y las
drogas vasoactivas y mantener un gasto cardiaco de 3L/min/m2.
Presiones
PAP elevadas podrán ser tratadas con hiperventilación para mantener pCO2 entre 30-35
y NO (óxido nítrico).
Mantener
este tipo de catéteres de forma prolongada (mas de 72 h) aumenta el riesgo de
infecciones.
Saturación venosa mixta
La Sat.VO2
se puede medir de forma continua con un catéter situado en la arteria pulmonar
en en la vena cava superior. Valores > 60% indican un adecuado gasto
cardiaco.
Pulsioxímetro
Monitoriza
la saturación de O2 transcutánea. Si la curva de pulso es sinosoidal
habrá dificultades de captación.
Temperatura
La perdida
de calor de estos pacientes es muy elevada ,debido al volumen de sangre que
circula por el circuito extracopóreo. La temperatura debe mantenerse entre
34º-36ºC. Si al paciente hay que enfriarle para mantener una FC óptima usaremos
una manta térmica con servorregulador.
Coagulación
Los pacientes
con asistencia ventricular están siempre anticoagulados, con una perfusión
continua de heparina sódica. Se mantendrán ACT (tiempo de coagulación activada)
entre 150-180 seg. Inicialmente se deben hacer controles cada 30 min. Para
luego seguir cada 3h. Es uno de los cuidados más importantes que hay que tener
con estos pacientes.
RIESGOS Y COMPLICACIONES DEL USO
DE VAD
Hemorragias
La
perfusión continua de heparina, los procedimientos quirúrgicos, cambios de
sistema, la canulación de grandes vasos aumenta considerablemente el riesgo de
hemorragias. Para evitarlas se deben mantener las plaquetas por encima de
100.000, realizando controles de hemograma c/ 12-24h. Valores de ACT > 180 seg. deben ser corregidos con la
disminución de la heparina y/o transfusión de plasma y plaquetas.
Hemólisis
El
hematocrito debe mantenerse entre 30-35 % ya que valores mas altos producen una
mayor hemólisis dentro del cono de la bomba al girar a velocidades de hasta
5000 rpm. Otro modo de prevenir la hemólisis es evitando que la temperatura
suba por encima de 37.5ºC.
Habrá que
vigilar la coloración de la orina por si apareciese hematuria, signo de alarma,
ya que puede inducir un fracaso renal agudo.
Tromoembolismo
Se intenta
evitar con la perfusión continua de heparina como anteriormente hemos
mencionado. La aparición de trombos suele producirse en las zonas de mayor
éxtasis venoso del sistema (cono). Un cambio en el zumbido de la bomba puede
indicar la existencia de algún trombo en el cono. Para evitar las complicaciones
tromboembólicas el
sistema se
cambia cada 3-4 días de forma rutinaria.
Infecciones
El tórax
abierto, los múltiples catéteres, los procedimientos quirúrgicos, las
transfusiones, la ventilación asistida, hace que estos pacientes sean particularmente
vulnerables a las infecciones. Su manejo debe ser con la más estricta asepsia
en cuanto a manipulación de vías, aspiración de secreciones, cura de heridas,
etc.
Es rutina
en nuestra unidad mantenerles con profilaxis antibiótica de amplio espectro:
Ceftazidima y Teicoplanina.
Fracaso
renal
En muchos
de estos pacientes el fallo renal ya está instaurado por el bajo gasto previo y
éste se mantiene o progresa durante la asistencia ventricular, precisando la
interposición de un hemofiltro en el asa arterial del sistema.
El
hemofiltro se coloca mediante un sistema en paralelo que permite cambiarlo
cuando sea necesario sin detener la VAD. La perfusión de heparina y el líquido
de reposición se ponen prefiltro para intentar prolongar la duración del
hemofiltro el mayor tiempo posible.
Estado
neurológico
Las
complicaciones neurológicas ocupan un lugar muy importante, el riesgo de
hemorragia intracraneal es alto. Son pacientes a los que se mantiene sedados y
relajados, dada su gran inestabilidad hemodinámica, por lo que para evaluar su
estado neurológico habrá que vigilar el estado de las pupilas regularmente. Si
existen dudas se puede realizar una “ventana anestésica” con la retirada
progresiva de relajantes y sedantes y EEG. La realización de otro tipo de pruebas
mas especificas y concluyentes que precisen un traslado (TAC) puede suponer un
gran riesgo. En nuestra experiencia ha
sido una de las causas principales para detener la asistencia.
PROBLEMAS
Y POSIBLES CAUSAS EN LVAD
|
PAI
PAI
PVC
PVC |
-Hipovolemia -Fallo Ventrículo dcho. -Soporte excesivo -Soporte inadecuado -Sobrecarga de volumen -Obstrucción cánula -Hipovolemia -CIA o foramen oval abierto -Sobrecarga de volumen -Insuficiencia ventrículo dcho. |
|
|
Flujo inadecuado Acidosis metabólica Hipoxia Hemorragia |
-Hipovolemia -Mala posición cánula -Trombosis en cánula o bomba -Acodamiento cánula -Soporte inadecuado -Hipovolemia -Daño hepático -Problema pulmonar -CIA o foramen oval abierto -Heparina alta -Hemorragia herida quirúrgica -CID |
Pedatric Cardiacac Intensive Care. Athony C. Chan.
Ed.98
SITUACIONES ESPECIALES
Cambio del
sistema de VAD
Es una
situación crítica que dura solo unos minutos pero durante los cuales el corazón
tiene que funcionar por si solo. Para realizar el cambio se debe tener
preparado sangre, plasma, volumen e inotrópicos. La técnica se realiza con
campo estéril, gorro, bata, mascarilla, etc.
Cambio de
hemofiltro
Al ir colocado el
hemofiltro en un sistema en paralelo el cambio no suele interferir en el
funcionamiento de la bomba. La técnica se realiza bajo normas estrictamente
asépticas. Las manipulaciones debe ser mínimas teniendo especial cuidado con el
purgado del sistema para evitar la entrada de aire, sobre todo si la asistencia
es izquierda.
RETIRADA DE LA
ASISTENCIA
El destete se realiza cuando se
dan las situaciones siguientes:
Aparición de onda pulsátil en la
presión arterial sistémica
Disminución de las necesidades de
inotrópicos
Posibilidad de disminuir el flujo
de la bomba manteniendo buena situación hemodinámica
Mejoría de la contracción
miocárdica por control ECO.
La retirada de la asistencia
ventricular se realiza siempre de forma progresiva optimizando las condiciones
de precarga y el inotropismo del paciente con expansión de volumen y aumento de
la perfusión de catecolaminas.
EXPERIENCIA
Tres pacientes en asistencia ventricular:
Miocardioptía
dilatada con fallo del VI
LVAD
durante 6 días
Interrupción por shock séptico
Truncus
arterioso trasplantado
RVAD 72 horas
Interrupción por fallo multiorgánico
CIV y TGA
con corrección anatómica
LVAD durante 14 días
Interrupción por hemorragia
intracraneal
CONCLUSIONES
La
asistencia ventricular forma parte del arsenal terapéutico en el tratamiento de
niños con cardiopatías congénitas y como puente al trasplante cardiaco.
Los
resultados iniciales están muy condicionados por la “curva de aprendizaje”.
Conocer esos parámetros y saber los
riesgos y complicaciones que se derivan
del uso de la asistencia ventricular es necesario para mantener unos cuidados
de enfermería adecuados para este tipo de pacientes.
BIBLIOGRAFÍA
Kimberly Scherr, RN, MN, Louise Jensen, RN, PhD, and Arvind Koshal, MD. American
Journal of Critical Care,Sep.99, Vol 8, No. 5, pp324-337.
DeBakey M. Left ventricular bypass pump for cardiac assistance: clinical
experience.
Am J Cardiol. 1971;27:3-11.
Jensen C., Hill CS. Mechanical support for congestive heart failure in infants and
children.
Crit Care Nurs Clin North Am. 1994
Mar;6(1):165-74.
Louis PT, Bricker JT, Frazier
OH, Duncan M, Towbin JA, Gelb BD, Macris MA, Radovencavic B, Kearney D, Igo S,
et al Nonpulsatile total left ventricular support in pediatric patients.
Crit Care Med. 1992 May;20(5):704-7.
Konertz W.,Reul H. Mechanical
circulatory support in children.
Int J Artif Organs. 1997
Dec;20(12):657-8.
Duncan BW,Hraska V, Jonas RA,
Wessel DL, del Nido PJ, Laussen PC, Mayer JE, Lapierre RA, Wilson JM.Mechanical
circulatory support in children with cardiac disease.J Thorac Cardiovasc Surg. 1999 Mar;117(3):529-42.
José M. Revuelta, Jesús Herreros. Avances en cirugía
cardiaca.
Pediatric Cardiac Intensive Care. Anthony C. Chan. Williams and Wilkins. Edición 1998
Conde Olasagasti JL, Amate Blanco JM, Alcaide Jiménez JF.
Informe sobre los dispositivos de asistencia ventricular como puente al
trasplante cardiaco. Revista española de trasplantes. May.97, vol.6, num.2