ENFERMERÍA BASADA EN LA EVIDENCIA:
MÉTODO CIENTÍFICO EN CIENCIAS DE LA
SALUD
Vicent
Modesto i Alapont (Pediatra)
UCIP/Rea. Servicio de Anestesia.
Hospital Infantil “La Fe”
Comisión de Medicina Basada en la
Evidencia
Hospital Universitari “La Fe”
(València)
En los años ochenta, los responsables del Programa de
Docencia para Residentes de Medicina Interna de la Facultad de Medicina de la
McMaster University de Ontario (Canadá) denominaron “Medicina Basada en la
Evidencia” (MBE) a una nueva estrategia de aprender y practicar la medicina que
ya llevaba desarrollándose durante una década en dicho centro[1]
y que fue luego adoptada por otros, entre ellos la Oxford University en
Inglaterra. Supone una revolución tan profunda que se ha considerado como un
“nuevo paradigma”[2] de la práctica clínica, y se enraíza
en la aplicación directa a la toma de las decisiones habituales en la labor
diaria de los profesionales de la salud (delante de un enfermo individual y
concreto), de los conocimientos derivados de las ciencias básicas
Bioestadística, Epidemiología Clínica y Metodología de la Investigación
Científica.
Para la MBE, la práctica médica correcta se sustenta en
la integración de dos pilares[3]:
el arte y la ciencia. El primero es la maestría y experiencia clínica
individual del médico, el dominio y el juicio que los clínicos desarrollan a lo
largo de su experiencia en la práctica. El segundo es el conocimiento
científico obtenido mediante el análisis sistemático y riguroso de las
mejores pruebas científicas disponibles en la literatura sobre ciencias de la
salud, especialmente de la investigación centrada en el paciente y referida a
la demostración de eficacia y seguridad de las intervenciones preventivas,
rehabilitadoras o terapéuticas, a la potencia de los marcadores pronósticos, y
a la exactitud y precisión de los tests diagnósticos. Queda desprestigiado el
conocimiento derivado sólo de la doctrina y el saber médico tradicional (lo que
“se ha hecho siempre”, lo que “pone en los libros”), de la “seducción” o en el
principio de autoridad (el valor de las opiniones de los colegas y maestros con
muchos años de experiencia y un asombroso “currículum”), o de la inducción
realizada con el sentido común y basada en la comprensión de las teorías
fisiopatológicas y los mecanismos básicos de la enfermedad (“tal medicación
seguro que funciona porque inhibe tal mecanismo de acción”).
La
práctica de la MBE se dio a conocer a la comunidad científica internacional en
19922, que la identificó como un enfoque
“maravillosamente refrescante” y pronto reconoció en ella la resurrección de la
llamada Médecine d’Observation practicada por Pierre Charles Alexandre
Louis y la Escuela de París hacia 1830[4] como reacción a la medicina especulativa.
A pesar de algunas críticas y reticencias iniciales[5],[6],
ha alcanzado una extraordinaria difusión, y su uso se ha generalizado gracias a
la serie Cómo mantenerse al día con la literatura médica[7],
las Guías para los usuarios de la literatura médica[8], la publicación del libro Medicina
Basada en la Evidencia: Cómo practicar y enseñar la MBE[9]
(que ha sido traducido al castellano y del que ya se han realizado dos
ediciones), la aparición de revistas especificamente dedicadas (Best
Evidence, Clinical Evidence,..), de centros e instituciones como la Colaboración
Cochrane, el Centre for MBE
del NHS Trust británico o el programa de talleres CASP (Critical
Appraisal Skills Program) y,
sobretodo, a la interminable lista de referencias al tema accesible mediante la
internet. Se ha estudiado el espectacular crecimiento de la MBE en la
literatura médica recogida en las bases de datos EMBASE (Excerpta
Medica/Elsevier)[10] y MEDLINE18 , y tanto Ellis[11]
como Gill[12] han comprobado
que actualmente el 80% de los pacientes atendidos tanto en hospitales como
ambulatorios reciben intervenciones avaladas por la mejor evidencia científica
disponible. Se considera que “en el siglo XXI el responsable de tomar
decisiones sobre la asistencia sanitaria tendrá que practicar la toma de
decisiones basada en la evidencia”[13].
En
España la MBE (cuya correcta denominación en castellano debería ser “Medicina
basada en Pruebas Científicas”[14])
también ha penetrado con fuerza y, por ejemplo, la prestigiosa revista Medicina
Clínica de Barcelona ha publicado ya dos suplementos especiales para
enseñar correctamente su uso[15],[16].
Los pediatras españoles, siguiendo las recomendaciones de nuestros colegas
norteamericanos[17],
consideramos ya a la “Pediatría Basada en la Evidencia” como un aprendizaje
imprescindible[18],[19],[20],[21].
La
fundadora de la enfermería profesional, Florence Nightingale, comprendió bien
la importancia del método científico. Analizando estadísticamente los datos
cuidadosamente recogidos durante la guerra de Crimea, publicó en 1859 su libro Notes
on Nursing en el que demostraba una
caída (del 42 al 2’2%) de la tasa de mortalidad de los soldados ingleses como
resultado de sus cuidados de enfermería, y también utilizó la estadística para
apoyar su argumento en pro de la reforma de los cuidados médicos en los
hospitales civiles y militares. Fue elegida miembro de honor de la Sociedad de
Estadística en 1860. A pesar de su ejemplo, la enfermería no ha sido
tradicionalmente una profesión “basada en evidencia”: Hunt[22]
y Camiah[23]
han objetivado que la mayoría de las prácticas de enfermería son rituales
asentados en la experiencia y la tradición.
En
1990, la S.E.E.C.I.P.N. organizó en València su XI REUNIÓN NACIONAL DE
ENFERMERIA DE CUIDADOS INTENSIVOS PEDIÁTRICOS Y NEONATALES, y la primera Mesa
Redonda versó sobre “Investigación en Enfermería”. Las principales conclusiones
fueron que la enfermería tiene mucho que aportar al conocimiento científico
para la resolución de los problemas de salud y enfermedad de los niños, y que
para ello la enfermería pediátrica debe realizar investigación científica
rigurosa y aprender a aplicar el saber derivado de esta investigación al
cuidado de los niños[24].
Curiosamente, ambas conclusiones han sido recientemente señaladas por dos de las
instituciones mas prestigiosas de la enfermería profesional, el International
Council of Nurses (ICN) y el National Institute of Nursing Research (NCNR),
como los objetivos más importantes de la investigación en enfermería[25].
Desde
entonces, y al amparo de la MBE, la enfermería de todo el mundo también ha
desarrollado la exigencia de una prestación sanitaria basada en fundamentos
rigurosos avalados científicamente[26].
Así ha surgido la “Enfermería Basada en la Evidencia” (EBE)[27],[28]:
en 1997 se celebra en Londres, bajo los auspicios del Royal Collage of Nursing
y la revista Nursing Standard, la “1st Nacional Conference on Evidence Based
Nursing”, y en 1998 aparece la revista Evidence Based Nursing. Hasta la
fecha se han identificado, en la literatura sobre áreas de la práctica de la
enfermería, 522 ensayos clínicos aleatorizados[29]
y 36 Revisiones Sistemáticas sobre efectividad[30].
Al
igual que en MBE, ante un problema concreto de la practica diaria de cuidados
de enfermería, la aplicación de la EBE sigue una serie de etapas:
1.-
Formulación de una pregunta estructurada y relevante. El problema concreto
(diagnóstico, pronóstico, etiología/factores de riesgo, aspectos
económicos,...) se traduce en una Pregunta que consta de 4 partes: Situación o
Población objeto, Intervención nueva a estudio o experimental, Intervención
habitual o control, Variables resultado o efecto como vamos a medir la
efectividad. Por ejemplo, una buena pregunta estructurada sería: ¿En RN
pretérmino que no se pueden alimentar por succión (Población objeto), la
colocación de una sonda orogástrica (experimental) frente a la sonda
nasogástrica (control) es mejor tolerada, medida en veces que se sale la sonda
o en días que pasan hasta que se alcanza la completa nutrición por vía
enteral,... (Resultado)?.
2.-
Búsqueda bibliográfica exhaustiva. Los usuarios de la EBE adquieren gran
destreza en el manejo de las bases de datos de literatura sanitaria (primarias
y secundarias) para recuperar toda la información relevante sobre el tema. El
uso de la informática es de gran apoyo durante esta fase.
3.-
Valoración crítica y rigurosa de los documentos recuperados. Es la fase más
característica del proceso. Los usuarios aprenden las “reglas de evidencia”,
una serie de conocimientos básicos en estadística y diseño de investigaciones,
mediante las cuales se hacen maestros en analizar críticamente la validez
científica de los artículos recuperados8. Desgraciadamente, la inmensa mayoría de los
trabajos carecen de rigor metodológico o de relevancia clínica, por lo que no
aportan conocimiento científico válido.
4.-
Aplicación de la mejor evidencia científica disponible al cuidado de nuestros
pacientes. En esta fase es en la que el conocimiento obtenido científicamente
es tamizado por la experiencia y el buen juicio del profesional sanitario, para
aplicarlo al cuidado de un paciente concreto, según sus especiales demandas y
valores, los recursos disponibles, sin olvidar el compromiso legal y ético que
implica toda intervención profesional. Posiblemente esta es la fase más
importante y difícil de todas.
5.-
Re-evaluar nuestro resultado para comprobar que la aplicación de la atención
sanitaria basada en evidencia esta mejorando la calidad de vida de nuestros
pacientes.
Para
la adquisición de las habilidades que implican todas estas etapas se han
publicado recientemente unas estupendas guías prácticas[31],[32],[33].
A pesar de que se han detectado una serie de problemas y dificultades en su
desarrollo[34], un
reciente meta-análisis[35]
de 84 estudios experimentales de intervenciones de enfermería (realizadas sin
que fuesen requeridas por el médico) demuestra que la EBE funciona: para la
práctica del cuidado de la salud, la aplicación de las medidas de enfermería
cuya efectividad se ha comprobado con investigaciones rigurosas es mejor que la
aplicación de medidas rutinarias o intervenciones control, pues mejoran el área
conductual, del conocimiento, fisiológica y psicológica de los pacientes.
Para
cimentar sólidamente el espectacular desarrollo que están actualmente
obteniendo las Prácticas Sanitarias “basadas en evidencia” (MBE, EBE, etc...)
nos parece muy adecuado que volvamos a los orígenes del problema y nos
planteemos de nuevo las preguntas fundamentales: ¿Cómo funciona el método
científico?, ¿Cómo somos capaces los humanos de obtener conocimiento sólido
acerca de la realidad del mundo de los fenómenos naturales?, ¿Son la Medicina y
la Enfermería una Ciencia?, ¿Cómo se aplica el método científico a las ciencias
de la Salud? o, mas prosaicamente, ¿Por qué debemos creer a los científicos y
no a los magos, curanderos o practicantes de medicinas alternativas?.
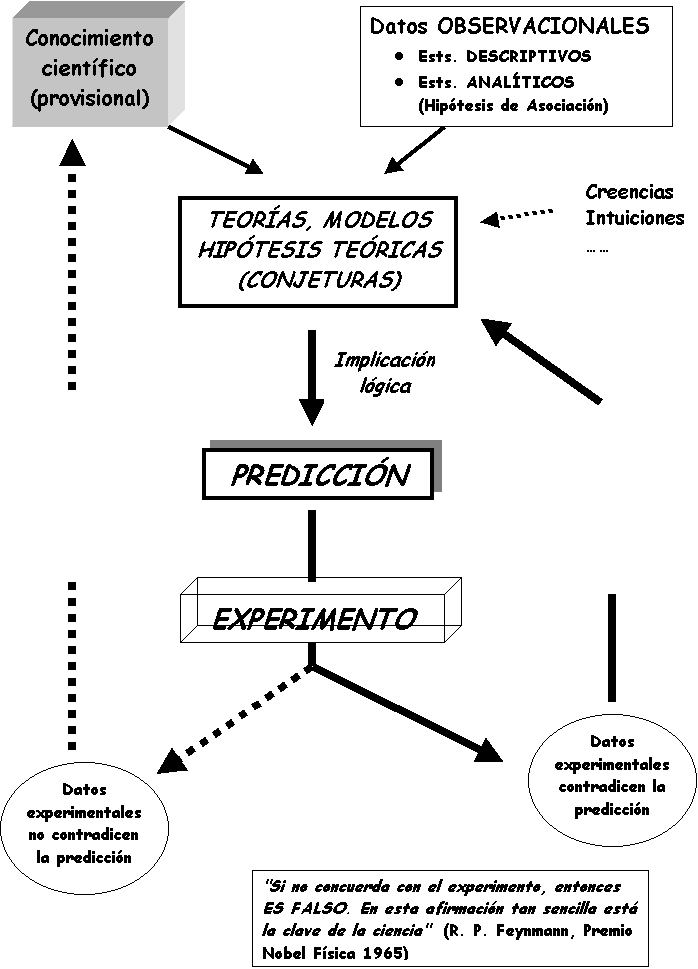
En
la conferencia de clausura de esta reunión intentaremos responder a estos
interrogantes estudiando sucintamente los fenómenos de la naturaleza y los
mecanismos lógicos mediante los cuales nuestra razón es capaz de establecer
conocimiento válido, para adentrarnos posteriormente en la descripción
detallada del método científico aplicado a las ciencias de la salud. Con todo
ello intentaremos demostrar que no debemos creer las predicciones y teorías a
las que no lleguemos mediante el método científico porque no sabemos qué
probabilidad tenemos de equivocarnos. Una afirmación se convierte en
verdad científica cuando el que la hace
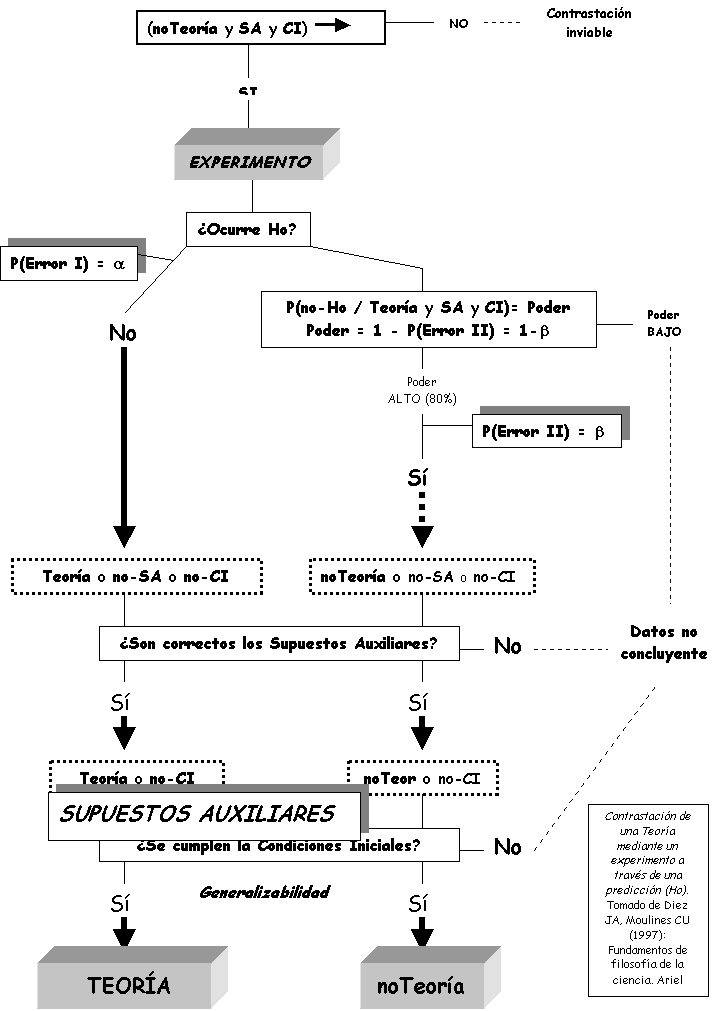
es capaz de cuantificar la probabilidad de que sea mentira[36].
Para estimar con rigor esta probabilidad debemos utilizar la estadística.


![]()
1.- VARIABLES ADECUADAS Y CÁLCULOS BIEN HECHOS:
Computadora
Condiciones
de aplicación de los test estadísticos
2.- REQUISITOS DE EXPERIMENTO ALEATORIO para que pueda
modelizarse por la estadística y la teoría de probabilidades (razonamiento
deductivo)
Distribución al azar pura (muestreo
aleatorio)
No pérdidas
en el seguimiento
Análisis según criterio de
"Intención de Tratar"
3.- REQUISITOS DE CAUSALIDAD
Sir A.B. Hill (1965) - U.S. Surgeon
General (1964-89)
4.- AUSENCIA DE ERROR SISTEMÁTICO (SESGOS)
Aleatorización y Muestra Grande (n>30-50)
Control de la
confusión e interacción (A. multivar.)
Enmascaramiento
Evitar sesgo
de selección (muestra no representativa)
Evitar sesgo
de información o de Clasif. Errónea
Evitar el
sesgo de publicación
5.- COMPARABILIDAD DE LOS GRUPOS
"La asunción básica de los diseños experimentales
es el control de todos los elementos extraños a la relación estímulo-respuesta:
que los grupos que se comparen sean idénticos, excepto en la intervención que
se evalúa. La mejor manera de conseguir la comparabilidad es la aleatorización:
si los grupos así obtenidos son comparables, cualquier diferencia observada
entre ellos al finalizar el experimento puede ser atribuida causalmente a la
intervención."
CRITERIOS DE CAUSALIDAD (Sir Austin B. Hill, 1965):
Relación CAUSA - EFECTO = Juicio de valor: "La mayoría de los estudios de investigación
clínica y epidemiológica tienen por objeto identificar la existencia de una
potencial relación causal entre el factor de estudio (exposición/tratamiento) y
la variable de respuesta (enfermedad/curación). No se trata, por tanto, de
determinar si existe una asociación matemática de ambas variables a nivel
poblacional, sino de establecer si ésta es del tipo causa-efecto, excluyendo todas las otras posibles
explicaciones alternativas de la relación observada."
1.- Estudio : Diseño adecuado + Validez Interna
2.- Criterios mayores
· Precedencia temporal correcta (E.
Prospectivo): Una intervención puede ser considerada causa de la
reducción en el riesgo de una enfermedad/anormalidad perinatal si, y sólo sí, aquella
se aplicó antes del momento en el que se desarrolló ésta
· Plausibilidad biológica: Un mecanismo biológicamente plausible debe ser capaz
de explicar por qué tal relación podría darse el caso de ocurrir
· Consistencia: Rara vez estudios únicos son definitivos. Resultados
concordantes aportados por varios estudios diferentes realizados en poblaciones
distintas y por investigadores diversos aportan más peso a la hipótesis de
causalidad. Si los resultados de varios trabajos son inconsistentes, debería estudiarse
primero la calidad metodológica de los estudios, pero no se excluye la
causalidad
· Exclusión de explicaciones
alternativas (Confusores): La
profundidad con la que se han estudiado posibles explicaciones alternativas es
un criterio importante a la hora de juzgar la causalidad
3.- Otros criterios
· Gradiente dosis-respuesta: Si un factor es efectivamente la causa de una
enfermedad, normalmente (aunque no invariablemente) a mayor exposición al
factor mayor riesgo de enfermedad. Tal relación dosis-respuesta no siempre
aparece, porque algunas importantes relaciones biológicas son dicotómicas y se
debe alcanzar cierto nivel umbral para observarse la respuesta.
La ausencia de este gradiente no excluye causalidad: su presencia la refuerza
· Magnitud de la fuerza de asociación
(RR/OR, DR) y Precisión de la estimación (IC estrecho)
· Efecto del cese de exposición: A no ser que exista un efecto mantenido, cuando una
intervención tiene un efecto beneficioso el beneficio debe desaparecer cuando
aquella se elimina de la población
U.S. Surgeon
General 1965: Smoking and Health
U.S Surgeon General 1990: Criteria for
evaluating evidence regarding the effectiveness of perinatal interventions
